3 V8 i1 G2 }- r5 O8 i7 I
第一章 “止痒平肤液”治疗表皮生长因子受体抑制剂相关中重度皮疹的随机、对照临床试验
$ z3 ] o% u' a- E) N8 B/ v$ h
第一节 概 述
9 M) B1 E( @7 g+ F1 eEGFRIs 相关皮疹的发生率很高,西妥昔单抗的Ⅲ期临床研究显示其相关的皮疹发生率可达88%~90%,是 EGFRIs 相关不良反应中发生率相对最高的一种。EGFRIs相关皮疹通常发生于如头面部和胸前等人体皮脂腺分布密集的部位,常常有瘙痒或疼痛等 伴随症状的发生,皮疹消退后遗留红斑或色素沉着的可能性也很大。指南推荐 EGFRIs相关皮疹的治疗以抗生素和激素为主,但疗效欠佳且抗生素和激素同样有着不小的副作用,通过中医药治疗 EGFRIs 相关皮疹成为解决这一难题的出路。本研究以 EGFRIs 相关中重度皮疹患者为研究对象,对“止痒平肤液”的疗效进行证实,同时对治 疗前后入组患者进行外周血液样本的留存,以用于后续试验的血清炎症因子变化情况检测,以期对“止痒平肤液”的作用机制展开初步的研究,为后续进一步的基础实验提供临床参考依据。
: K0 N7 R2 d- _$ j
课题来源:
北京市卫计委首都卫生发展科研专项项目——外用中药“止痒平肤液”治疗中重度靶向药相关皮疹的前瞻、随机、对照临床研究
$ T. C, g7 J; g
第二节研究对象与方法
1 p6 l T1 m5 h$ l/ s
/ H u- s8 d8 j9 p9 @
1.试验设计
本研究采用随机、对照、双盲的试验设计方法。
, Z6 L9 @0 r% `5 }5 P2 L9 C
1.1 患者来源
选取2018年11月至2020年12月期间,就诊于中日友好医院门诊或病房的患者。
' r5 A% U5 a8 r$ A9 M8 [
1.2 随机和盲法
研究分组用的随机表由与本试验完全无关的专业统计人员使用 SAS9.4 统计软件生 成,并据此将入组患者随机分入试验组或对照组,受试者本人和研究人员均不知道被纳 入的组别。请第三方将药物按照随机表统一进行编码并封存盲底,研究人员按照编码发放药物。试验结束后统一揭盲。
" V. V d3 O1 l$ \8 q
1.3 样本量计算
样本量计算采用优效设计方案,以有效率为主要评价指标。通过文献检索发现应用 西药标准治疗方案治疗 EGFRIs 相关皮疹的有效率最高约为63.33%。令α=0.05,β= 0.1,采用双侧检验,依据样本量计算公式计算得出的样本量为47例。取样本量50例, 考虑到20%的脱落比例,最后试验的总样本量取60例,试验组和对照组每组各30 例。两独立样本率的优效检验公式(1)如下:
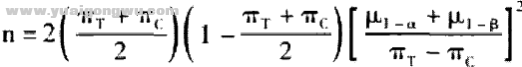 ( H+ d; G' ^$ B9 D
( H+ d; G' ^$ B9 D
2. 诊断标准
2.1 西医诊断标准
EGFRIs 相关皮疹的诊断标准:1.患者接受 EGFRIs 治疗;2.用药后出现皮疹;3.皮疹表现为痤疮样或脓疱样,分布在皮脂腺旺盛区域,伴有瘙痒。EGFRIs 相关皮疹的分级应用癌症支持疗法多国协会 (multinational association of supportive care in cancer,MASCC)制定的EGFRIs相关皮肤不良反应MASCC分级标准,见表1:
& X* ?0 t" p1 J6 v
: W/ R- e- m0 u" |# F# M
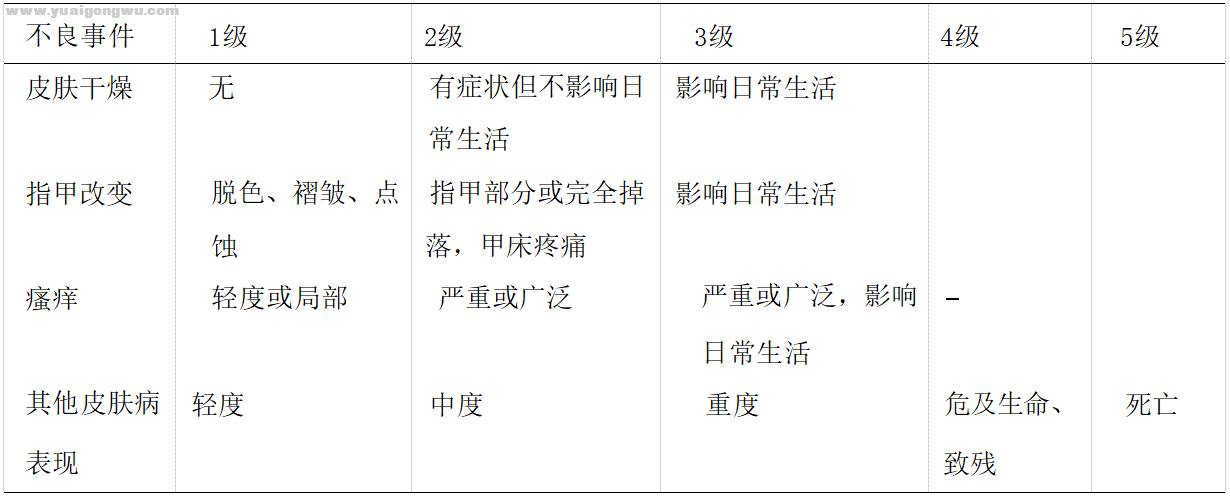
其他 EGFRIs相关的皮肤不良反应(如 EGFRIs 相关的皮肤瘙痒、皮肤干燥和甲沟 炎)的分级,应用美国国家癌症研究所 (National Cancer Institute,NCI) 制定的常见不良反应事件评价标准 (Common Terminology Criteria for Adverse Events,CTCAE) 进行评价和分级[19],见表2:
! A) L) {- x8 b, P6 B4 w
5 X _- J# ~: F: r9 q 2.2中医诊断标准
EGFRIs 相关皮疹的中医诊断标准:风热型:痤疮样皮疹伴有瘙痒,面红目赤,舌色淡红或红。湿热型:脓疱样皮疹,伴有口苦,小便黄,舌红苔黄。
9 U! A* [% W; G" K+ g6 E3 z
3.纳、排标准
$ i8 j; {* ~, B& t+ v
3.1 纳入标准
(1)经病理诊断为恶性肿瘤;
(2)正在使用 EGFRIs 类药物,并出现 EGFRIs 相关皮疹;
(3)年龄≥18岁,卡氏评分 (KPS)≥60 分,预计生存期≥3个月;
(4)皮疹分级符合MASCC 分级标准2级(中度)或2级以上,且症状持续一天以上;
(5)无智力及精神障碍,语言表达能力可,能配合进行症状评价及生活质量评分;
(6)患者签署知情同意书。
( x4 w" S: E% D8 M
3.2 排除标准
(1)已停止 EGFRIs 治疗;
(2)未出现皮疹或皮疹分级为 MASCC分级标准1级(轻度);
(3)同时患有其他皮肤疾病;
(4)存在其他严重的并发症,如严重心、肝、肾功能衰竭等;
(5)过敏体质;
(6)依从性差。
2 i$ y3 Z& x" e2 X/ K/ T. B$ Z
3.3 脱落标准
(1)由于病情进展或其他原因,停止使用 EGFRIs 的患者;
(2)由于自身或外界原因,未应用试验用药的患者;
(3)使用了除本试验之外其他治疗EGFRIs 相关皮疹药物的患者。
& G" {' k8 t. S0 U+ `8 ~; u) l, T. r
4.治疗方案
& L u1 V2 [. L% L# h
试验组:外用“止痒平肤液”联合西医标准治疗。
对照组:外用安慰剂联合西医标准治疗。
7 G9 G2 a# G2 c9 D% ?3 s7 q
西医标准治疗方案为 EGFRIs 相关皮肤毒性临床实践指南中推荐的治疗方法:中度皮疹患者外用氢化可的松乳膏同时口服米诺环素,重度皮疹患者在外用氢化可的松乳膏联合米诺环素口服的基础上,加用甲泼尼龙口服。
- Q5 [, g6 j' |5 P2 Y$ Y
“止痒平肤液”及安慰剂使用方法:将“止痒平肤液”或安慰剂药液倒于空白面膜 上,外敷于皮疹密集处,若皮疹为散发或局部不宜外敷面膜,则可将药液直接涂于皮疹处。每日2次,每次30分钟,使用后用清水洗净,以免中药液残留导致色素沉着,连续应用14天。“止痒平肤液”及安慰剂均由中日友好医院制剂室生产加工,安慰剂与试验用药的外观、气味等各方面均一致。
$ G. h3 {7 |5 [$ m! M
丁酸氢化可的松乳膏使用方法:外用,涂抹于皮疹处,每日2次,连续应用14天,天津金耀药业有限公司提供。
& b8 I I6 _: Y- [7 z5 [+ W
盐酸米诺环素胶囊使用方法:口服,每日2次,每次100mg,口服14天。当患者出现严重消化道反应或皮疹减轻至轻度时,可经研究者确认后减量或停药。惠氏制药有限公司提供。
1 \* ^6 F& {% q* e
甲泼尼龙片使用方法:口服,每日1次,每次20mg, 口服14天。当患者出现严重不良反应或皮疹减轻至轻度时,可经研究者确认后减量或停药。辉瑞制药有限公司提供。
/ f+ y2 q$ m4 A& y- l# |
5.观察方法
5.1 观察方法
入组时对患者进行详细的问诊、查体,记录原始病历。根据 MASCC 标准对入组患 者的皮疹进行分级,并在保护患者隐私的前提下对患者的皮疹部位进行拍照留存。于入 组第7天和第14天时对患者进行随访,依据 MASCC 标准对皮疹进行再次分级,并对
皮疹部位进行拍照比较。
/ ^% ?: R( _1 F/ h- f! A- B* E! {
5.2 标本采集
所有入组患者分别于入组时和入组第7天留取外周静脉血标本5mL,静置10 min后于中日友好医院临床研究所肿瘤科实验室离心10min(2000 转/min), 于 2mLEP 管中注入离心后的上层血清,加盖后使用封管膜封好,标号并冻存于临床研究所肿瘤科-80℃冰箱内。入组患者于入组当天的前后3天内和入组后第14天的前后三天内进行血常规和肝功能、肾功能相关指标的检测。
. T$ v2 W$ x: U+ P0 F
6.疗效评价指标
! z& o- H; S3 d; q
6.1 主要疗效评价指标
2 u7 X; r* l" r2 h$ E: {
EGFRIs 相关中重度皮疹的治疗有效率。
m3 O2 [0 O0 z
依据美国 EGFRIs 相关皮肤毒性研讨会共识制定的疗效评价标准进行患者疗效评价,将疗效分为痊愈、好转和无效三种。
2 Y0 Y- Y H( e$ {
痊愈即患者被评价的皮肤不良反应消失,没有主观症状,没有感染征象,可正常进 行生活和工作。好转即患者被评价的皮肤不良反应分级下降一级及以上,或患者皮肤不良反应分布由广泛变为局部、患者的主观自觉症状减轻或消失、患者的生活质量评分较 前明显改善。无效即患者被评价的皮肤不良反应较治疗前无变化,或皮肤不良反应分级 较前上升,或患者皮肤不良反应分布由局部变为全身广泛分布、患者出现新发主观症状或原有主观症状加重、患者生活质量明显恶化。
; U$ C: L! P O% x: Y
治疗的总有效率即治疗后疗效评价为痊愈和好转的病例数之和,占该组入组总例数的百分比,即总有效率=(痊愈+好转)/总例数×100%。
% ]8 ?1 S9 C) A5 x% x" M
6.2 次要疗效评价指标
6 B* N5 H5 o1 s* e
6.2.1 皮疹伴随的瘙痒症状评分。
8 B7 m! G b7 c" A. ~. W/ Z: D
6.2.2 EGFRIs其他皮肤不良反应分级。皮肤干燥、甲沟炎等。
& _# w9 P& Q5 r7 h
6.2.3 米诺环素和甲泼尼龙用量。
7 M' e3 I2 b6 e( Z9 a8 E
6.2.4 生活质量
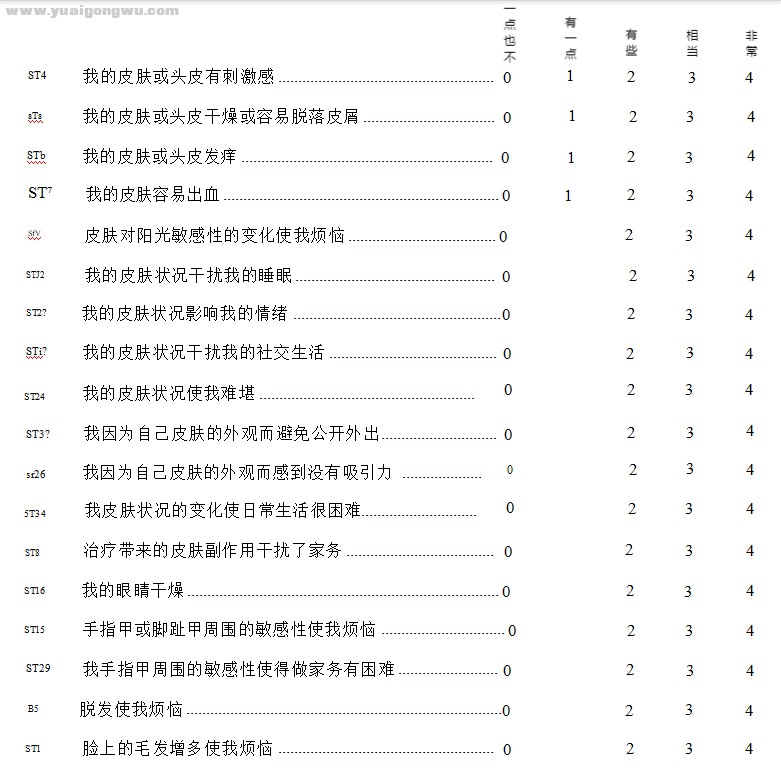
应用EGFRIs相关的癌症治疗功能评估问卷(Functional Assessment of Cancer Therapyquestionnaire-EGFRI, FACT-EGFRI-18)21]进行评价,见图1:
1 j/ ^* P* B- g! Z
 + t+ B0 a# N/ m
+ t+ B0 a# N/ m
6.3 安全性指标
' c( X; K2 T( Z6 z
所有患者于入组前和全部入组治疗结束后各抽取外周血标本进行一次血常规和肝 功能、肾功能的检测,以用于评估试验的安全性。并对试验过程中发生的各种不良事件
进行记录。
3 q! N5 t+ G1 c' ^% O
7. 统计分析
统计分析应用 SPSS 20.0软件进行。计数资料采用百分比的形式表示,并应用卡方 检验进行组间比较;对于计量资料采用均数±标准差(π±s)的形式表示,当数据符合正态分布时,依据方差齐性检验的结果,组间比较时应用独立样本t检验或 t'检验,组内比较时应用配对样本t检验或t检验;数据不符合正态分布时,应用 Wilcoxon 秩和检验。所有的统计分析均采用双侧检验,当P≤0.05 时认为所检验的差异之间存在统计学意义。
, x i- U0 H% Y4 U
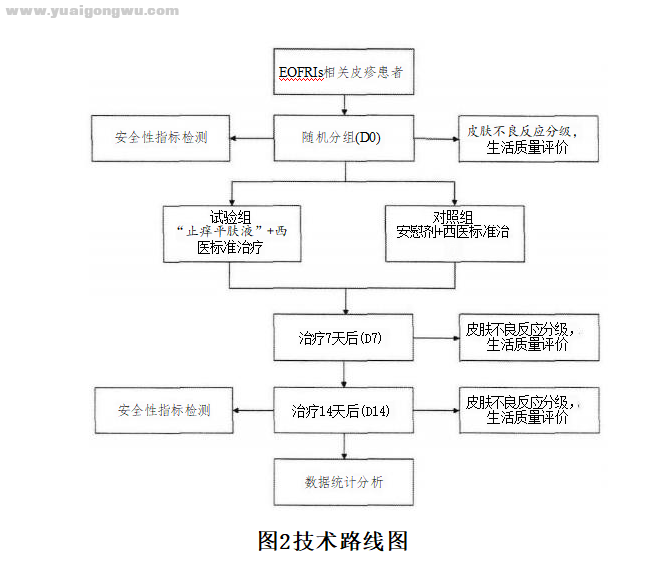
8.技术路线
 % r9 S3 W3 D0 R# R. L: o) |" H
% r9 S3 W3 D0 R# R. L: o) |" H
* M+ c0 |) X- Q1 |" r张静怡. “止痒平肤液”治疗EGFRIs相关中重度皮疹的RCT研究及作用机制探讨[D].北京中医药大学,2022.
w* h, s+ m& |/ S
7 z" U2 {0 b# X, _; X, C, g